مقالات, مقالات باتری و UPS
باتری دانیل ساختمان و کار سلول باتری دانیل
در این مقاله قصد داریم در مورد باتری دانیل صحبت کنیم.
فهرست مطالب
1- باتری دانیل چیست؟
2- ساختمان سلول دانیلی
3- اصول کار سلول دانیلی
1- باتری دانیل چیست؟
باتری دانیل سلول دانیلی نسخه اصلاح شده پیل ولتاییاست.
اشکال قطبی سازی پیل ولتایی در یک سلول دانیل حل شدهاست و میتواند به عنوان یک نسخه بهبود یافته از پیل ولتایی در نظر گرفتهشود.
ساختمان سلول دانیل کاملاً سادهاست.
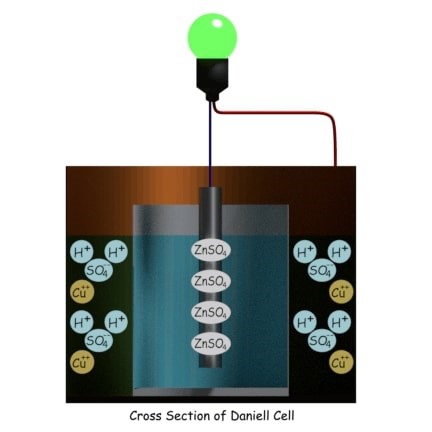
2- ساختمان سلول دانیلی
ساختمان سلول دانیلی شامل یک ظرف مسیاست که با یک محلول غلیظ سولفات مس پر شدهاست.
در داخل ظرف، یک گلدان استوانهای متخلخل پر از اسید سولفوریک رقیق قرار گرفتهاست که در محلول غلیظ سولفات مس غوطه وراست.
یک میله آمالگام روی اسید سولفوریک رقیقشده در گلدان متخلخل فرو میرود.
از نظر خاصیت الکترولیتهای رقیق، اسید سولفوریک به شکل رقیقشده آن با یونهای هیدروژن مثبت و یون سولفات منفی وجوددارد.
یونهای سولفات با میلههای روی تماسیافته و به میله الکترون آزاد میکنند و از طریق واکنش اکسیداسیون سولفات روی تولید میکنند.
در نتیجه میله روی بار منفی میگیرد و مانند کاتد رفتار میکند.
یونهای هیدروژن مثبت می توانند از دیواره متخلخل گلدان عبورکرده و در محلول سولفات مس بیایند و در آنجا با یونهای سولفات الکترولیت سولفات مس بپیوندند و اسید سولفوریک را تشکیل دهند.
یونهای مثبت مس الکترولیت سولفات مس با دیواره داخلی ظرف مسی در تماس هستند و در آنجا الکترون از دست میدهند و به اتمهای مسی تبدیل میشوند و روی دیواره رسوب میکنند.
3- اصول کار سلول دانیلی
بگذارید اصول کار سلول و باتری دانیل را به صورت گام به گام برای درک بهتر توضیح دهیم.
در محلول رقیق اسید سولفوریک یونهای H + و SO4– – وجود دارد.
یونهای H+ از طریق دیواره گلدان متخلخل به محلول سولفات مس میرسند.
یونهای سولفات اسید سولفوریک رقیقشده با میله روی واکنش نشان میدهند که یونهای روی Zn++ با یونهای SO4— به هم میچسبند و سولفات روی را تشکیل میدهند(ZnSO4) .
در طی این واکنش اکسیداسیون ، هر اتم روی دو الکترون را در میله روی قرار میدهد. از این رو میله روی منفی میشود و این بدان معنیاست که مانند کاتد باتری رفتار میکند.
یونهای هیدروژن(H+) در محلول سولفات مس تشکیل اسید سولفوریک (H2SO4) می دهند و یونهای مس (Cu++) به دیواره محفظه مس خارجی میآیند.
یونهای مس با گرفتن الکترون از ظرف دیواره ظرف مسی به عنوان فلز رسوب میکنند.
در نتیجه، ظرف مسی بار مثبت میگیرد به این معنی که این ظرف ، آند سلول دانیلی است.
اکنون اگر یک اتصال خارجی بین میله روی مرکزی و الکترونهای دیگ ظرف مسی را به یکدیگر وصل کنیم، جریان برق از میله روی به ظرف مس شروع به جاری شدن میشود. باتری دانیل
در سلول دانیلی، ما میتوانیم از نقطه ضعف قطبیشدن که اصلی ترین نقطه ضعف پیل ولتاییاست، جلوگیری کنیم.
از آنجا که گاز هیدروژن روی آند رسوب نمیکند زیرا قبل از رسیدن به آند (دیواره ظرف مسی) اسید سولفوریک تشکیل میدهد،
هیچ لایهای از هیدروژن روی آند ایجاد نمی شود تا مانع از کاهش واکنش شود.
مقالات مرتبط:
پیل ولتایی(سلول ولتايي) ساختار و نحوه ی کار آن
انواع مختلف پیل و باتری و کاربردهای آنها